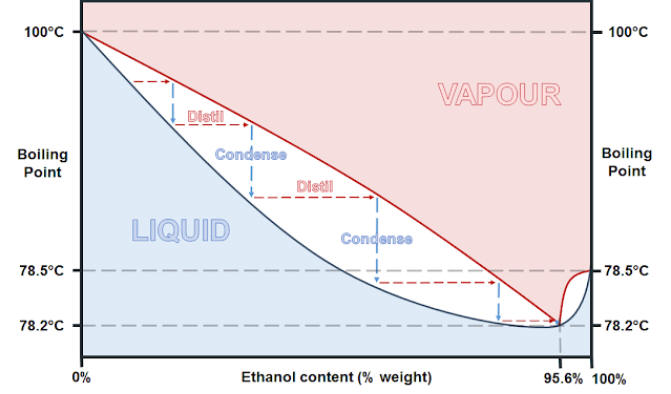

Le procédé utilise la différence de volatilité (capacité à s'évaporer selon la température) entre les constituants afin de les séparer : le composé le plus volatil s'évaporera plus facilement et composera la majeure partie des vapeurs. Il est ainsi possible de créer une phase gazeuse ayant une composition différente du mélange initial. Par condensation de ces vapeurs, un liquide appelé distillat peut être récupéré avec une concentration élevée du composé le plus volatil.
Le distillat n'est pas un produit pur : il contient une certaine proportion des autres composés du mélange initial. Il faut dès lors répéter l'opération d'évaporation-condensation avec le distillat afin de concentrer davantage le composé le plus volatil. Pour ne pas répéter l'opération, et séparer proprement les composants du mélange en une seule passe, on utilise une colonne de distillation et ce procédé se nomme distillation fractionnée ou rectification.
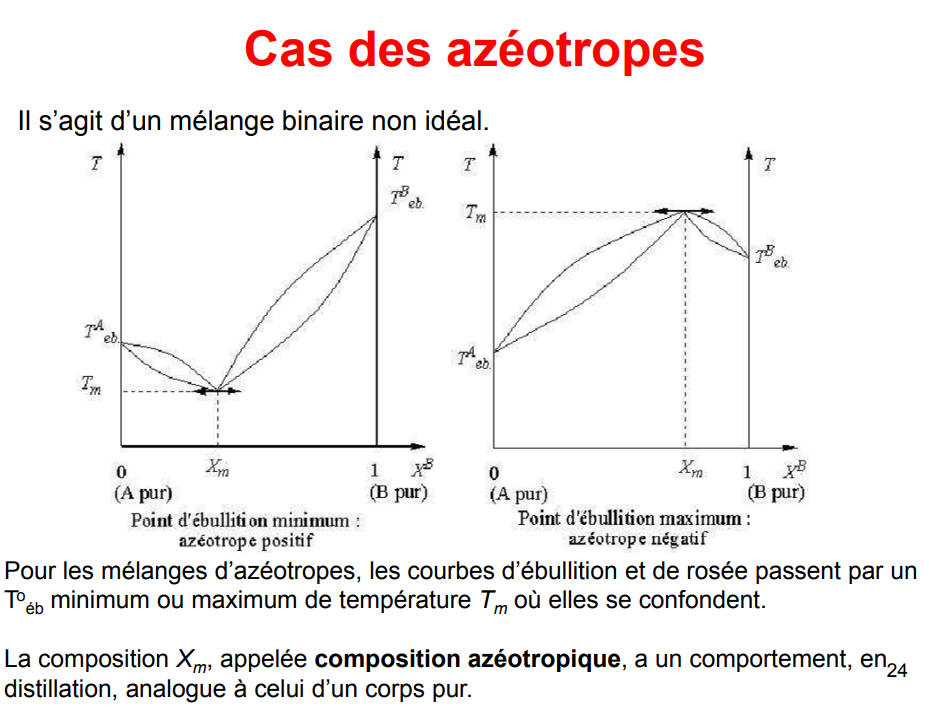
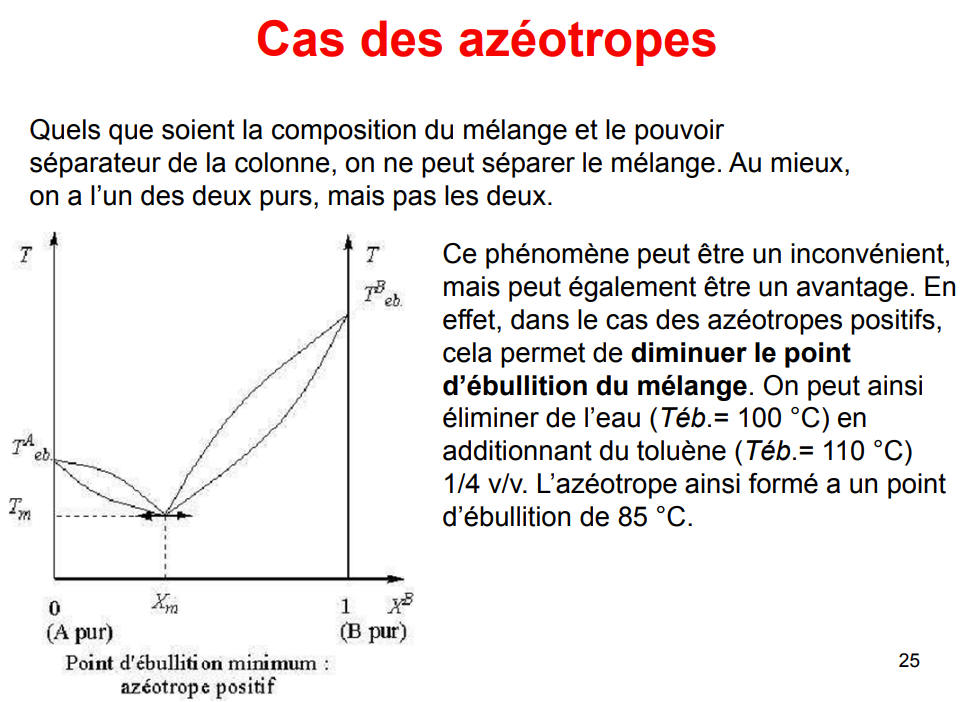
En fonction des propriétés physiques des constituants, il arrive que des composés aient des volatilités constantes par rapport au mélange initial, et que les vapeurs d'un tel mélange gardent toujours la même composition même si on répète l'opération évaporation-condensation plusieurs fois. Il s'agit d'un mélange azéotropique qui nécessite des conditions spéciales afin de séparer les composants (voir distillation azéotropique).
La distillation peut être effectuée de plusieurs manières : discontinue, continue, sous vide
I. Principe
La distillation est une technique de séparation de liquides dans un mélange
homogène. Les liquides sont vaporisés les
uns à la suite des autres par ordre de température d’ébullition croissante. Ils
sont récupérés dans des récepteurs
distincts.
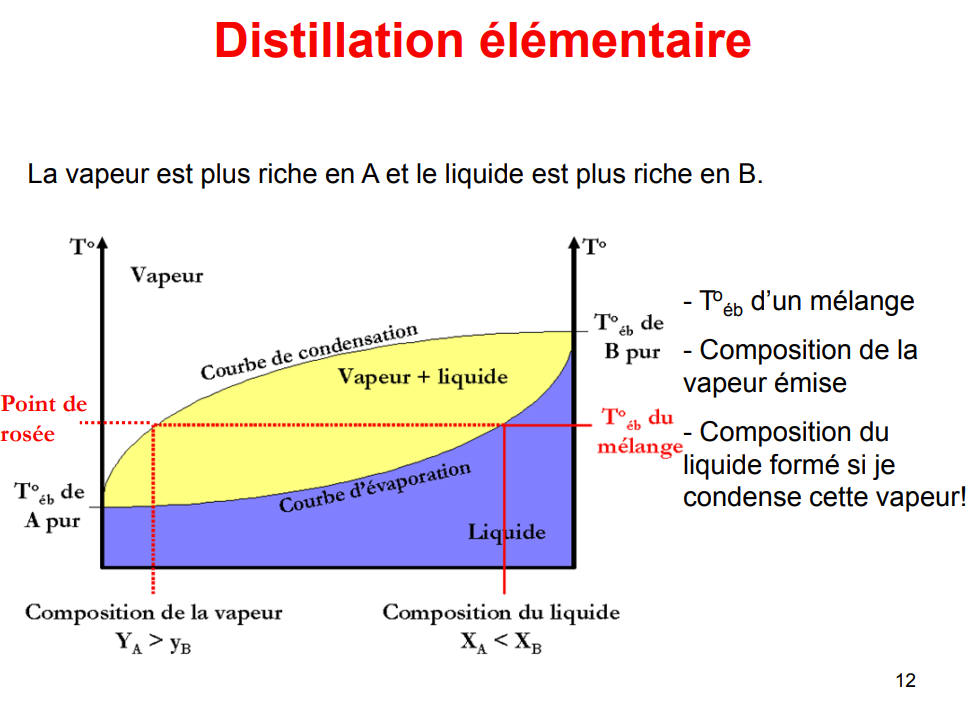
1. Distillation simple (ou élémentaire)
L’appareil est monté sans colonne. Le distillat est le produit d’une seule
séquence vaporisation - condensation.
Par distillation simple on élimine un solvant volatil dans lequel est dissous un
solide ou un liquide peu volatil.
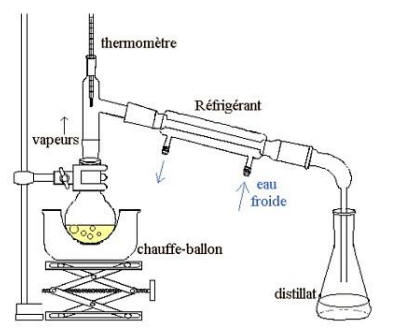
2. Distillation fractionnée (ou rectification)
L’appareil est monté avec une colonne à distiller (colonne de Vigreux).
La rectification permet :
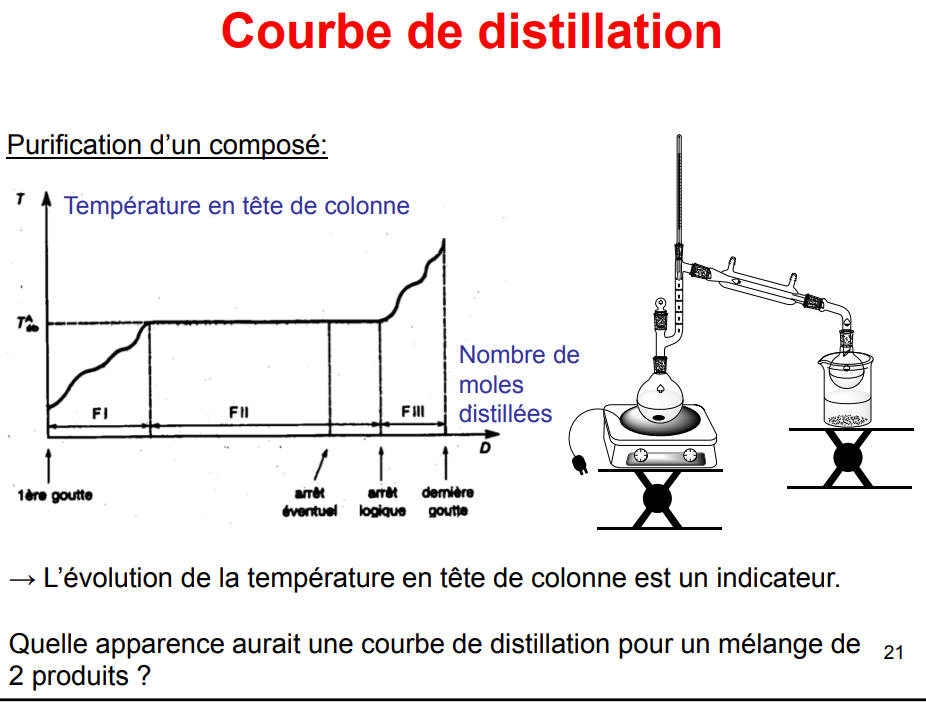
▫ La purification d’un composé
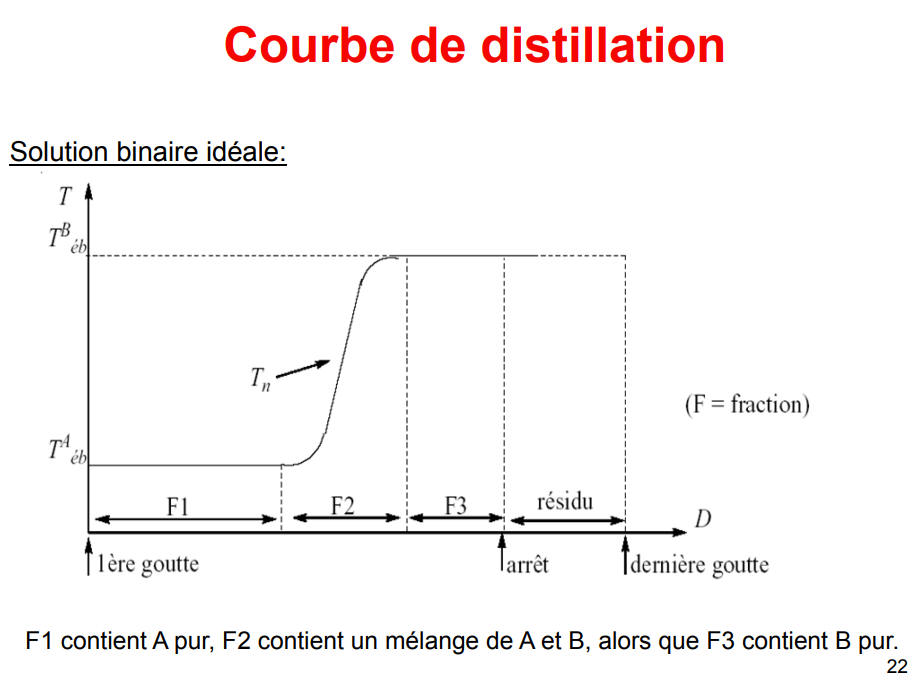
▫ L’isolement des constituants d’un mélange
▫ Le déplacement d’un équilibre par élimination d’un
produit de la réaction.
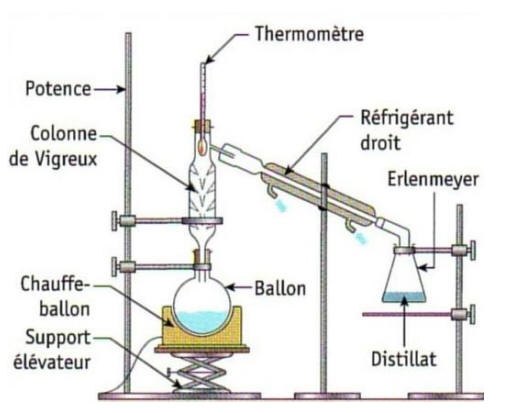
3. Distillation sous pression réduite
En abaissant la pression, on diminue la température d’ébullition d’un liquide.
La réalisation d’une distillation fractionnée sous pression réduite est plus
complexe qu’une distillation sous pression
atmosphérique. Elle présente néanmoins plusieurs avantages :
▫ Distiller des composés dont le point d’ébullition sous pression atmosphérique
est supérieur à 180 °C.
▫ Distiller des produits qui se dégradent à la chaleur ou qui s’oxydent à l’air.
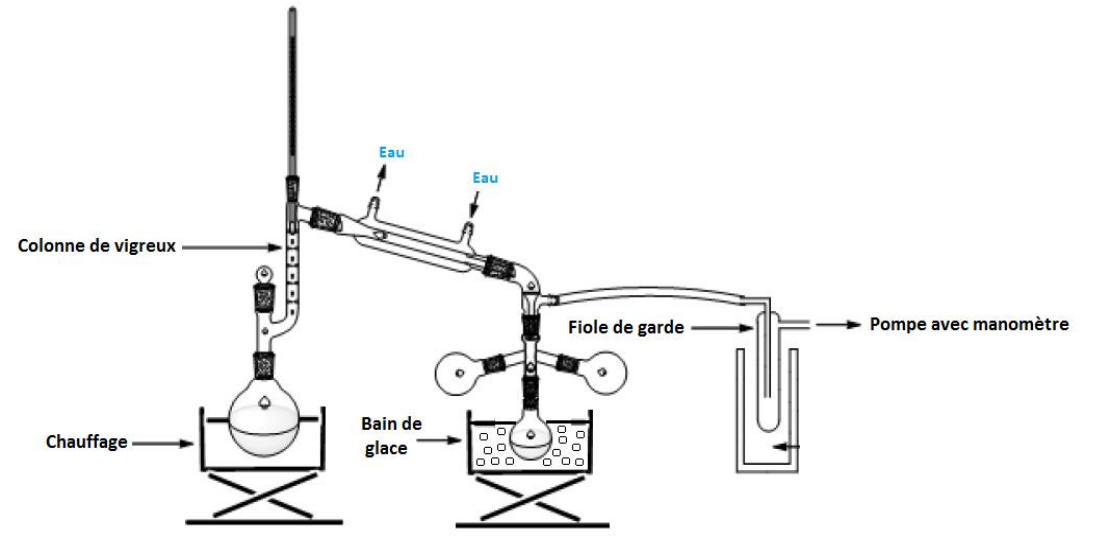
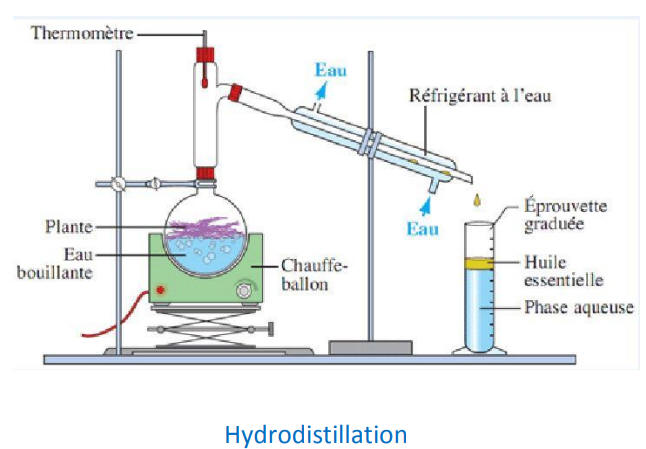
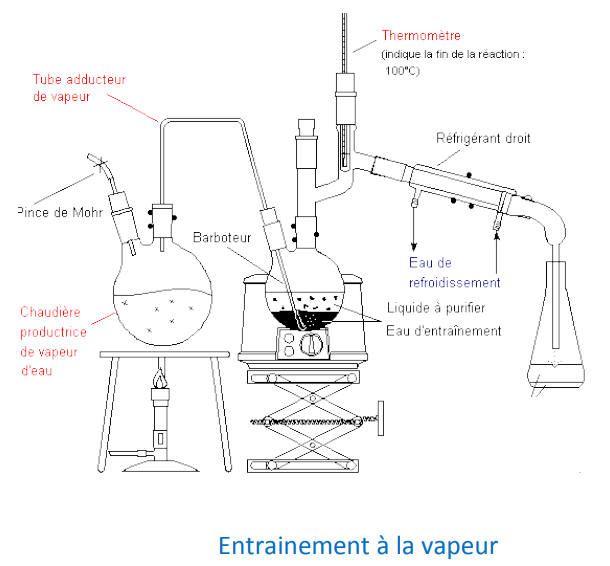
4. Hydrodistillation et entraînement à la vapeur
L’hydrodistillation et l’entrainement à la vapeur sont deux techniques basées
sur la distillation d’un mélange
hétérogène eau-composé organique.
Les applications principales sont :
▫ L’isolement des huiles essentielles des plantes
▫ L’isolement d’un composé organique situé dans un milieu très hétérogène.
II. Aspects expérimentaux
1. Réguler l’ébullition
Afin de réguler l’ébullition, il est nécessaire d’introduire de la pierre ponce
qui favorise la création de bulles d’air au sein
du mélange réactionnel. Des billes de verre peuvent être aussi utilisées.
2. Réglage du débit
La qualité de la séparation dépend du régime de distillation. Il faut maintenir
un régime régulier car les à-coups de
chauffage, de reflux ou de prélèvement entraînent une baisse importante de la
stabilité des équilibres
thermodynamiques et donc du pouvoir séparateur de la colonne.
3. Repérage des différentes fractions
Les différentes fractions distillées peuvent être identifiées par réfractométrie,
spectroscopie IR ou UV, chromatographie
sur couche mince…
L’observation de la température en tête de colonne est une méthode
d’identification peu précise. Elle permet
néanmoins d’avoir une première information sur le liquide distillé.
4. Arrêt de la distillation
Pour des raisons de sécurité, il faut toujours laisser une petite quantité de
résidu dans le bouilleur
![]()
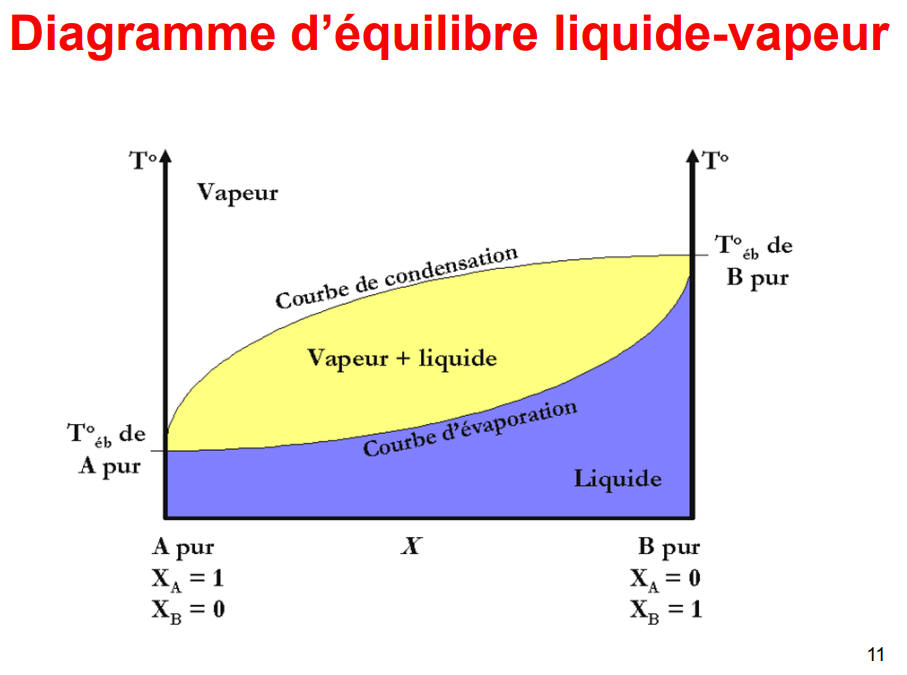
En vase clos: Un liquide enfermé en vase clos est toujours en présence de sa vapeur. Il y a un équilibre entre le liquide et la vapeur émise par celui-ci, appelé vapeur saturante P0.



![]()